Vaak is er een probleem om te bepalen welke van de elektroden de kathode is en welke de anode. Eerst moet u de voorwaarden begrijpen.
Het concept van kathode en anode - een eenvoudige uitleg
In complexe stoffen zijn elektronen ongelijk verdeeld tussen atomen in verbindingen. Als gevolg van de interactie verplaatsen deeltjes zich van een atoom van de ene stof naar een atoom van een andere. De reactie wordt redox genoemd. Het verlies van elektronen wordt oxidatie genoemd en het element dat elektronen afstaat, wordt een reductiemiddel genoemd.
Het toevoegen van elektronen wordt reductie genoemd, het ontvangende element in dit proces is het oxidatiemiddel. De overdracht van elektronen van het reductiemiddel naar het oxidatiemiddel kan via een extern circuit plaatsvinden en kan vervolgens worden gebruikt als een bron van elektrische energie.Apparaten waarin de energie van een chemische reactie wordt omgezet in elektrische energie worden galvanische cellen genoemd.
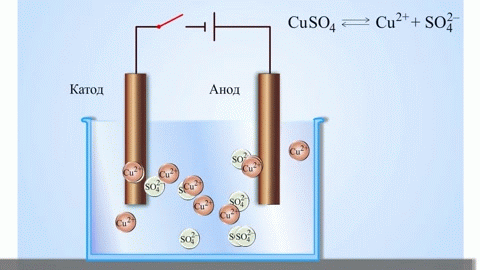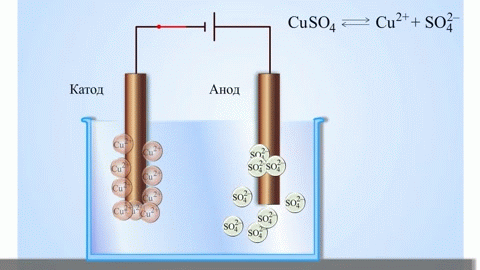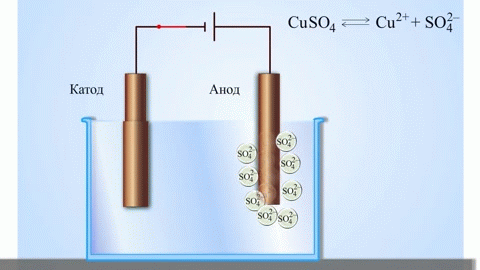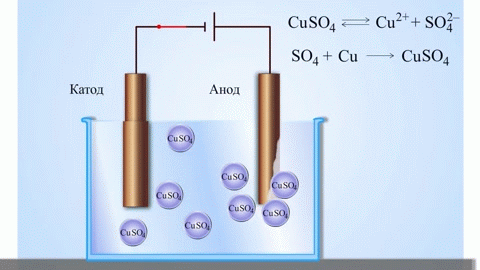
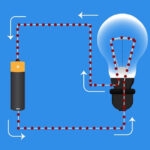
Het eenvoudigste klassieke voorbeeld van een galvanische cel zijn twee platen gemaakt van verschillende metalen en ondergedompeld in een elektrolytoplossing. In een dergelijk systeem vindt oxidatie plaats op het ene metaal en reductie op het andere.
BELANGRIJK! De elektrode waarbij oxidatie optreedt, wordt de anode genoemd. De elektrode waarop de reductie plaatsvindt, is de kathode.
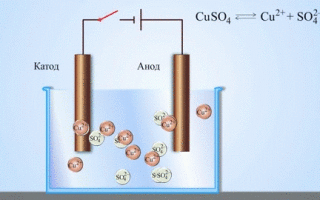
Uit schoolboeken voor scheikunde is een voorbeeld bekend van een koper-zink galvanische cel, die werkt door de energie van de reactie tussen zink en kopersulfaat. In het Jacobi-Daniel apparaat wordt een koperen plaat in een kopersulfaatoplossing (koperelektrode) geplaatst, een zinkplaat wordt ondergedompeld in een zinksulfaatoplossing (zinkelektrode). De zinkelektrode geeft kationen af aan de oplossing, waardoor er een overmatige positieve lading in ontstaat, en bij de koperelektrode is de oplossing uitgeput in kationen, hier is de oplossing negatief geladen.
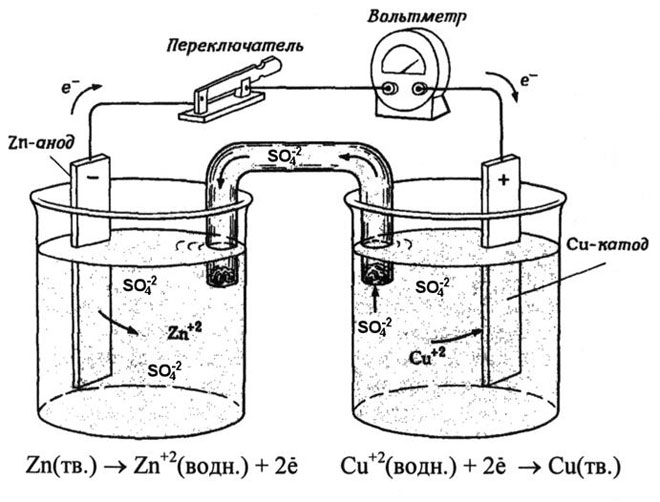
Het sluiten van het externe circuit zorgt ervoor dat elektronen van de zinkelektrode naar de koperelektrode stromen. Evenwichtsrelaties aan de fasegrenzen worden onderbroken. Er vindt een oxidatie-reductiereactie plaats.
De energie van een spontane chemische reactie wordt omgezet in elektrische energie.
Als een chemische reactie wordt uitgelokt door externe energie van een elektrische stroom, vindt een proces plaats dat elektrolyse wordt genoemd. De processen die plaatsvinden tijdens elektrolyse zijn het omgekeerde van de processen die plaatsvinden tijdens de werking van een galvanische cel.
AANDACHT! De elektrode waar de reductie plaatsvindt wordt ook wel de kathode genoemd, maar is bij elektrolyse negatief geladen, terwijl de anode positief geladen is.
Toepassing in de elektrochemie
Anodes en kathoden nemen deel aan veel chemische reacties:
- Elektrolyse;
- Elektroextractie;
- galvaniseren;
- Elektrotype.
Metalen worden verkregen door elektrolyse van gesmolten verbindingen en waterige oplossingen, metalen worden gezuiverd van onzuiverheden en waardevolle componenten worden geëxtraheerd (elektrolytische raffinage). Platen worden gegoten uit het te reinigen metaal. Ze worden als anodes in de elektrolyseur geplaatst. Onder invloed van een elektrische stroom ondergaat het metaal ontbinding. De kationen gaan in oplossing en worden afgevoerd bij de kathode, waarbij een afzetting van puur metaal wordt gevormd. De onzuiverheden in de originele ongereinigde metalen plaat blijven ofwel onoplosbaar als anodeslib of gaan in de elektrolyt waar ze worden verwijderd. Koper, nikkel, lood, goud, zilver, tin worden onderworpen aan elektrolytische raffinage.
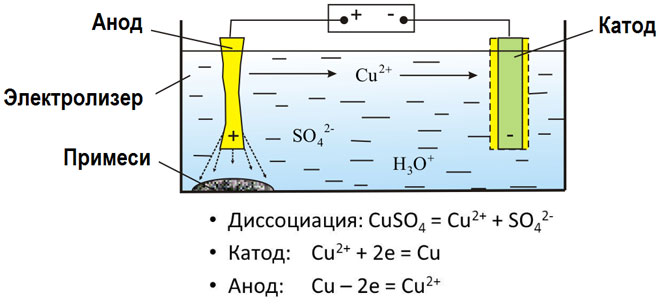
Elektro-extractie is het proces van het scheiden van een metaal uit een oplossing tijdens elektrolyse. Om het metaal in oplossing te brengen, wordt het behandeld met speciale reagentia. Tijdens het proces wordt een zeer zuiver metaal neergeslagen bij de kathode. Zo worden zink, koper, cadmium verkregen.
Om corrosie te voorkomen, om sterkte te geven, om het product te versieren, is het oppervlak van het ene metaal bedekt met een laag van het andere. Dit proces wordt galvaniseren genoemd.

Galvaniseren is het proces van het verkrijgen van metalen kopieën van bulkvoorwerpen door elektrolytische afzetting van metaal.

Toepassing in vacuüm elektronische apparaten
Het werkingsprincipe van de kathode en anode in een vacuümapparaat kan worden gedemonstreerd door een elektronenlamp.Het ziet eruit als een hermetisch afgesloten vat met metalen onderdelen erin. Het apparaat wordt gebruikt om elektrische signalen te corrigeren, te genereren en om te zetten. Volgens het aantal elektroden zijn er:
- dioden;
- triodes;
- tetroden;
- pentoden, enz.
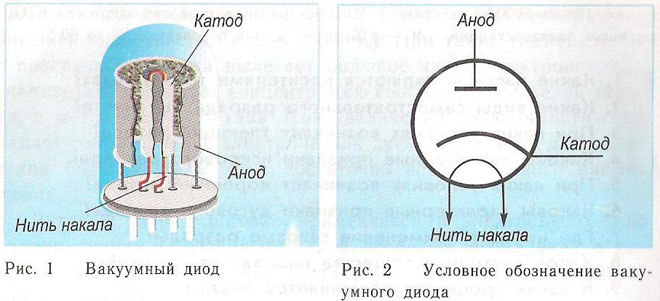
Een diode is een vacuümapparaat met twee elektroden, een kathode en een anode. De kathode is verbonden met de negatieve pool van de stroombron, de anode - met de positieve. Het doel van de kathode is om elektronen uit te zenden bij verhitting door een elektrische stroom tot een bepaalde temperatuur. De uitgezonden elektronen creëren een ruimtelading tussen de kathode en de anode. De snelste elektronen haasten zich naar de anode en overwinnen de negatieve potentiaalbarrière van de ruimtelading. De anode ontvangt deze deeltjes. In het externe circuit wordt een anodestroom gecreëerd. De elektronische stroom wordt geregeld door extra elektroden door er een elektrisch potentiaal op aan te leggen. Door middel van diodes wordt wisselstroom omgezet in gelijkstroom.
Toepassing in elektronica
Tegenwoordig worden diodes van halfgeleiders gebruikt.
In de elektronica wordt de eigenschap van diodes om stroom in de voorwaartse richting door te laten en niet om in de tegenovergestelde richting door te geven, veel gebruikt.
De werking van de LED is gebaseerd op de eigenschap van halfgeleiderkristallen om te gloeien wanneer een stroom door de pn-overgang in voorwaartse richting wordt geleid.
Galvanische gelijkstroombronnen - batterijen
Chemische bronnen van elektrische stroom waarin omkeerbare reacties plaatsvinden, worden batterijen genoemd: ze worden opgeladen en herhaaldelijk gebruikt.

Tijdens de werking van een loodaccu treedt een redoxreactie op.Metallisch lood oxideert, geeft zijn elektronen af, waardoor looddioxide wordt verminderd, dat elektronen accepteert. Het loodmetaal in een batterij is de anode en is negatief geladen. Looddioxide is een kathode en is positief geladen.
Terwijl de batterij ontlaadt, worden de stoffen van de kathode en anode en hun elektrolyt, zwavelzuur, verbruikt. Om de batterij op te laden is deze aangesloten op een stroombron (plus op plus, min op min). De richting van de stroom is nu het omgekeerde van wat het was toen de batterij werd ontladen. Elektrochemische processen op de elektroden zijn "omgekeerd". Nu wordt de loodelektrode de kathode, het reductieproces vindt erop plaats en het looddioxide wordt de anode, waarbij de oxidatieprocedure plaatsvindt. De batterij herschept de stoffen die nodig zijn voor zijn werking.
Waarom is er verwarring?
Het probleem ontstaat doordat een bepaald ladingsteken niet stevig op de anode of kathode kan worden bevestigd. Vaak is de kathode een positief geladen elektrode en de anode een negatieve. Vaak, maar niet altijd. Het hangt allemaal af van het proces dat plaatsvindt op de elektrode.
AANDACHT! Het deel dat in de elektrolyt wordt geplaatst kan zowel de anode als de kathode zijn. Het hangt allemaal af van het doel van het proces: je moet er nog een laag metaal op leggen of verwijderen.
Hoe de anode en kathode te identificeren?
In de elektrochemie is de anode de elektrode waarop oxidatieprocessen plaatsvinden, de kathode is de elektrode waar reductie plaatsvindt.
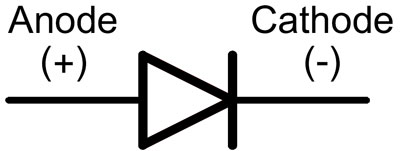
In een diode worden de aftakkingen een anode en een kathode genoemd. De stroom zal door de diode vloeien als de anode-aftakking is aangesloten op de "plus", de "kathode" -aftakking - op de "min".
Bij een nieuwe LED met ongeknipte contacten worden de anode en kathode visueel bepaald op lengte. De kathode is korter.

Als de contacten zijn afgesneden, kan een eraan bevestigde batterij helpen. Licht zal verschijnen wanneer de polariteiten overeenkomen.
Anode en kathode teken
In de elektrochemie is het juister om niet te praten over de tekenen van de ladingen van de elektroden, maar over de processen die erop plaatsvinden. De reductiereactie vindt plaats aan de kathode en de oxidatiereactie vindt plaats aan de anode.
In de elektrotechniek is voor de stroomtoevoer de kathode verbonden met de negatieve pool van de stroombron, de anode met de positieve.
Vergelijkbare artikelen: